Man mano che l'acqua si raffredda, il suo comportamento diventa, da un punto di vista fisico, sempre più strano.
Secondo i risultati di un nuovo studio condotto da un team di ricercatori dell’Università di Stoccolma sembrerebbe aver trovato qualcosa di nuovo nel comportamento dell’acqua, un “punto critico” precedentemente nascosto che compare nell'acqua sovraraffreddata (acqua che non congela pur trovandosi a temperature inferiori a 0°C).
 Immagine 1 - Un team internazionale di ricerca coordinato dal team di scienziati del dipartimento di Fisica dell'Università di Stoccolma è riuscito a manipolare gli stati dell’acqua attraverso l’utiilzzo di fasci di luce laser a raggi X (Credit image POSTECH University, South Korea).
Immagine 1 - Un team internazionale di ricerca coordinato dal team di scienziati del dipartimento di Fisica dell'Università di Stoccolma è riuscito a manipolare gli stati dell’acqua attraverso l’utiilzzo di fasci di luce laser a raggi X (Credit image POSTECH University, South Korea).
Attraverso diverse combinazioni di pressione e temperatura gli scienziati sono in grado di mantenere l'acqua in forma liquida ben al di sotto del normale punto di congelamento. In alcune ricerche precedenti (tra cui uno studio realizzato in maniera congiunta da ricercatori dell’Università Sapienza di Roma e Università di Birmingham, Regno Unito pubblicato sulla rivista Nature Physics nel 2022 https://www.nature.com/articles/s41567-022-01698-6 ) i ricercatori avevano teorizzato che, in questa fase speciale, l'acqua si separava in due fasi distinte sia come liquido ad alta densità sia come liquido a bassa densità.
In questo nuovo studio, un team internazionale di ricercatori ha ottenuto dati che sembrano evidenziare in maniera più diretta l’esistenza sia di questo stato “liquido-liquido” sia di un punto critico oltre il quale l'acqua passa a uno stato unico, ma volatile, in relativamente alla propria struttura molecolare.
Ottenere una visione approfondita di questi stati dell'acqua si è rivelato alquanto difficile, perché tali stati esistono proprio al confine tra l'acqua che congela e si trasforma in ghiaccio. I vari tentativi per ottenere misurazioni accurate di tale transizione sono stati descritti da alcuni ricercatori come “terra di nessuno”.
«La particolarità del nostro lavoro è data dal fatto che siamo stati in grado di colpire il ghiaccio con il laser a raggi X così velocemente prima ancora che il ghiaccio si congelasse e abbiamo potuto osservare in che modo la transizione “liquido-liquido” scompare lasciando il posto a un nuovo stato critico» scrive il chimico-fisico Anders Nilsson dell'Università di Stoccolma, Svezia.
«Per decenni si sono avute speculazioni e sono state elaborate diverse teorie per spiegare queste proprietà straordinarie. Una di queste teorie ipotizzava l'esistenza di un punto critico. Ora sappiamo che tale punto esiste» continua il ricercatore svedese.
Il riscaldamento rapido (tramite laser a infrarossi) e lampi super-veloci (tramite laser a raggi X) sono stati fondamentali per gli esperimenti condotti dagli scienziati svedesi. I ricercatori hanno prodotto il ghiaccio e lo hanno fatto transitare sia attraverso lo stato “liquido-liquido” sia attraverso il punto critico mantenendolo nello stato fluttuante mentre contemporaneamente effettuavano tutte le misurazioni necessarie su scale di tempo microscopiche.
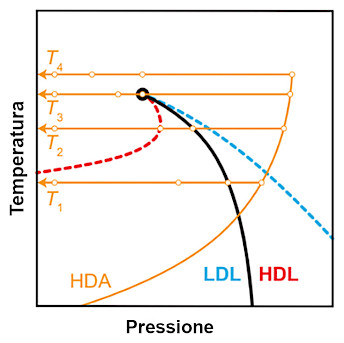 Immagine 2 - I ricercatori hanno studiato in che modo le variazioni di temperatura e pressione modificavano il ghiaccio amorfo ad alta densità (HDA, high-density amorphous ice), il liquido a bassa densità (LDL, low-density liquid) e il liquido ad alta densità (HDL, high-density liquid). Credit image: Seonju You et al., Science, 2026.
Immagine 2 - I ricercatori hanno studiato in che modo le variazioni di temperatura e pressione modificavano il ghiaccio amorfo ad alta densità (HDA, high-density amorphous ice), il liquido a bassa densità (LDL, low-density liquid) e il liquido ad alta densità (HDL, high-density liquid). Credit image: Seonju You et al., Science, 2026.
Anche se il punto critico esatto non è stato ancora trovato questo studio restringe significativamente i confini del problema. I ricercatori ipotizzano che lo stato critico si manifesti intorno a una temperatura di -63 °C e a una pressione di 1000 atm (atmosfere, questa ipotesi aiuterà nel condurre ulteriori studi specifici.
Inoltre se dovessimo fare un paragone il punto critico sembra essere simile a un buco nero. Man mano che l'acqua si avvicina ad esso la dinamica del sistema del liquido rallenta e i cambiamenti nella struttura richiedono molto più tempo. Questo rende impossibile per il liquido evitare la transizione.
Queste scoperte a prima vista potrebbero sembrare esoteriche e interessare soltanto i fisici ma, in realtà, ci aiutano a capire meglio in che modo l'acqua “agisce” (e perché può “comportarsi” in modi così strani) a livello fondamentale. Ciò ha implicazioni in quasi tutte quelle situazioni in cui è coinvolta l'acqua sul nostro pianeta e non solo.
«I ricercatori che studiano la fisica dell'acqua possono ora concordare sul modello secondo cui l'acqua ha un punto critico nel regime sovraraffreddato» sostiene Nilsson.
«La fase successiva della ricerca è comprendere le implicazioni di questi risultati sull'importanza dell'acqua nei processi fisici, chimici, biologici, geologici e climatici» prosegue il ricercatore svedese.
Basta guardare i cubetti di ghiaccio per vedere quanto sia strana l'acqua. In generale quando la materia si raffredda, si contrae e diventa più densa ma non l'acqua, questo è il motivo per cui i cubetti di ghiaccio galleggiano in cima a un bicchiere invece di affondare sul fondo.
Esistono molte altre proprietà strane dell'acqua oltre ai suoi stati più comuni, incluso il comportamento liquido “due-in-uno” analizzato nello studio svedese. Si tratta di un altro passo avanti ma lo studio lascia aperte ancora molte domande a cui dare risposta.
Un'altra cosa che distingue l'acqua dagli altri liquidi è che rappresenta un elemento essenziale per la vita, per quanto ne sappiamo. Questa è una direzione che i ricercatori vogliono continuare a esplorare.
«Trovo molto emozionante il fatto che l'acqua sia l'unico liquido supercritico a condizioni ambientali che rende possibile la vita e sapere che quando manca non c'è vita» dice il fisico chimico Fivos Perakis, dell'Università di Stoccolma. «Si tratta di una pura coincidenza o c'è qualche conoscenza essenziale ancora da acquisire?» conclude Perakis.
Lo studio “Experimental evidence of a liquid-liquid critical point in supercooled water” ha visto la collaborazione dei ricercatori di Svezia, Germania, Corea e Canada ed è stato pubblicato sulla rivista Science https://doi.org/10.1126/science.aec0018



 Identificata formazione cristalli di sale grazie a video a livello atomico
Identificata formazione cristalli di sale grazie a video a livello atomico Scoperto nuovo tipo di legame chimico ultra forte?
Scoperto nuovo tipo di legame chimico ultra forte? Batteria al litio e CO2?
Batteria al litio e CO2? Come ottenere acqua potabile dall'aria
Come ottenere acqua potabile dall'aria Fotosintesi artificiale per produrre idrogeno combustibile
Fotosintesi artificiale per produrre idrogeno combustibile