All’origine della SLA un “errore” di comunicazione tra muscolo e nervo
Lo studio, coordinato dalla Sapienza, è pubblicato su Antioxidant and redox signaling (Ars)
Lo studio coordinato da Antonio Musarò del Dipartimento di Scienze anatomiche, istologiche, medico-legali e dell’apparato locomotore della Sapienza, con la collaborazione di Fondazione Roma, IIT-Sapienza, Istituto Pasteur-Italia e Telethon, ha individuato il meccanismo molecolare responsabile dello smantellamento della giunzione neuromuscolare (NMJ) che si verifica in molte patologie e alterazioni patologiche.

Le giunzioni neuromuscolari sono la regione di comunicazione tra muscolo e nervo e rappresentano un vero e proprio ponte funzionale; infatti, ricevendo input fisiologici e patologici dai due tessuti, muscolo e nervo, consentono agli stessi di funzionare e comunicare in modo corretto.
Nel quadro degli studi finora condotti, volti principalmente all’individuazione dei meccanismi patogenici caratterizzanti della sclerosi laterale amiotrofica (SLA), rimaneva irrisolto il problema se lo smantellamento delle NMJ fosse un evento riconducibile direttamente a livello delle cellule nervose (neuroni motori) o se possa verificarsi indipendentemente dalla loro degenerazione.
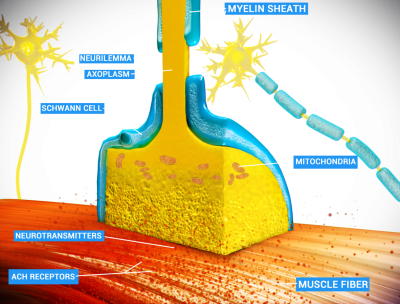 Image - A neuromuscular junction (or myoneural junction) is a chemical synapse formed by the contact between a motor neuron and a muscle fiber. It is at the neuromuscular junction that a motor neuron is able to transmit a signal to the muscle fiber, causing muscle contraction. Credits: By Doctor Jana - http://docjana.com/#/nmj, CC BY 4.0, https://commons.wikimedia.org/w/index.php?curid=46835961
Image - A neuromuscular junction (or myoneural junction) is a chemical synapse formed by the contact between a motor neuron and a muscle fiber. It is at the neuromuscular junction that a motor neuron is able to transmit a signal to the muscle fiber, causing muscle contraction. Credits: By Doctor Jana - http://docjana.com/#/nmj, CC BY 4.0, https://commons.wikimedia.org/w/index.php?curid=46835961
Lo studio condotto dalla Sapienza e pubblicato sulla rivista internazionale Antioxidant and redox signaling (Ars), ha tentato di rispondere a questa domanda. Il gruppo di ricerca ha realizzato un modello sperimentale nel quale è stata indotta in topi un’alterazione genica – simile a quella che si verifica nei pazienti affetti da SLA familiare – selettivamente nei muscoli, quindi senza coinvolgere i neuroni motori. L’obiettivo era quello di indagare se una alterazione che parte dal muscolo potesse compromettere il “mantenimento” della giunzione neuromuscolare e quindi della comunicazione muscolo-nervo.
“Abbiamo dimostrato – afferma Musarò – che una alterazione del muscolo scheletrico induce uno smantellamento della giunzione neuromuscolare. Abbiamo quindi individuato il meccanismo molecolare alla base dello smantellamento e scoperto che questo dipende dall'attivazione di una proteina chinasi, conosciuta come PKC theta.
Conseguentemente, un suo “silenziamento” farmacologico ha permesso di preservare le giunzioni neuromuscolari e di promuovere un mantenimento della massa e forza muscolare nei topi trattati.
"Il nostro lavoro – conclude Musarò – supporta il concetto del "dying back", per cui una alterazione a livello periferico può portare all'attivazione di meccanismi degenerativi a livello “primario”, nei neuroni motori; propone inoltre un nuovo approccio terapeutico per trattare la SLA e patologie neuromuscolari, attivando un processo di "saving back".
Riferimenti:
Muscle Expression of SOD1G93A Triggers the Dismantlement of Neuromuscular Junction via PKC-Theta - Gabriella Dobrowolny, Martina Martini, Bianca Maria Scicchitano, Vanina Romanello,Simona Boncompagni, Carmine Nicoletti, Laura Pietrangelo, Simone De Panfilis, Angela Catizone,Marina Bouché, Marco Sandri, Rudiger Rudolf, Feliciano Protasi, and Antonio Musarò – Antioxidant and redox signaling; DOI:10.1089/ars.2017.7054
